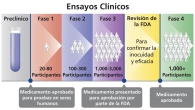
Solicitud de autorización de un nuevo medicamento en fase de investigación clínica
Solicitud de aprobación presentada por un patrocinador farmacéutico a la Administración de Alimentos y Medicamentos (FDA) de los Estados Unidos para someter a prueba un medicamento en fase de investigación clínica en sujetos humanos (ensayos clínicos fase 1 a 4). La revisión de esta solicitud por la FDA asegura que el medicamento es inocuo para prueba en sujetos humanos y que la prueba no someterá a los sujetos del estudio a un riesgo irrazonable.
Download Glossary
-
Versión en inglés PDF(3.13MB)
-
Versión en Español PDF(3.16MB)